เจ็ตพลาสมาอากาศเพื่อบำบัดแผลติดเชื้อเรื้อรัง: จาก “ฟิสิกส์” สู่ “การแพทย์” “บำบัดแผล” ด้วย “พลาสมาเย็น”
ในโลกยุคปัจจุบันจำนวนผู้ป่วยแผลเรื้อรัง เช่น แผลเบาหวาน (diabetic ulcers), แผลกดทับ (pressure ulcers) และแผลเรื้อรังที่ขาจากโรคหลอดเลือดดํา (venous leg ulcers) ได้เพิ่มขึ้นอย่างต่อเนื่อง[1,2] การหายของแผลที่ช้านั้นนำมาสู่การเพิ่มภาระในการดูแลผู้ป่วยเหล่านี้ ต้องใช้บุคลากร อุปกรณ์และงบประมาณทางการแพทย์จำนวนมาก นอกจากนี้การหายของแผลที่ช้ามีโอกาสทำให้เกิดการติดเชื้อที่รุนแรงและนำไปสู่การตัดอวัยวะ ส่งผลกระทบต่อรายได้ของครอบครัวและระบบเศรษฐกิจของประเทศ[3–5]
กระบวนการหายของแผล (wound healing) [5–8] เป็นกระบวนการอันซับซ้อนที่ร่างกายทำการซ่อมแซมเนื้อเยื่อหรือผิวหนังที่ได้รับความเสียหาย โดยปกติแบ่งเป็น 3 ระยะที่เกิดต่อเนื่องทับซ้อนกัน ประกอบด้วย
(1) ระยะการอักเสบ (inflammation phase) ซึ่งประกอบด้วยกระบวนการสำคัญ คือ การห้ามเลือด (hemostasis) การกำจัดเซลล์ที่ตาย เศษเซลล์และแบคทีเรียในแผล
(2) ระยะการเจริญของเนื้อเยื่อใหม่ (proliferation phase) ประกอบด้วยกระบวนการสำคัญ คือ การสร้างหลอดเหลือดใหม่ (angiogenesis) การวางตัวของคอลลาเจน (collagen deposition) การสร้างเนื้อเยื่อแกรนูเลชั่น (granulation tissue formation) การสร้างเนื้อเยื่อบุ (epithelialization) และการหดของบาดแผล (wound contraction)
(3) ระยะการปรับเปลี่ยนรูปร่าง (remodeling phase) ซึ่งเป็นระยะแผลปิดสนิทและมีการปรับเปลี่ยนรูปร่างใหม่ของคอลลาเจนให้มีความแข็งแรงมากกว่าเดิม หากกระบวนการหายของแผลนี้ถูกรบกวนหรือขัดขวางด้วยปัจจัยต่างๆ เช่น การบาดเจ็บซ้ำ (repeated or continuous injury) การติดเชื้อยืดเยื้อ (persistent infection) เนื่องจากมีแบคทีเรียและไบโอฟิล์ม และการขาดเลือดไปเลี้ยงบริเวณแผล (ischemia) ปัจจัยเหล่านี้จะทำให้แผลอยู่ในระยะการอักเสบที่ยาวนานกว่าปกติ หน่วงกระบวนการหายของแผลและนำไปสู่การเป็นแผลเรื้อรัง[9,10]
พลาสมาเย็นความดันบรรยากาศ (cold/low-atmospheric pressure plasmas) คือ พลาสมาที่สามารถผลิตขึ้นในดวามดันบรรยากาศ (1 atm) และมีอุณหภูมิของพลาสมา ณ ขณะที่สัมผัสกับพื้นผิวใดๆ โดยเฉพาะผิวชีวภาพ ไม่เกิน 40 ๐C [11] เพื่อหลีกเลี่ยงอันตรายที่เกิดจากความร้อน การผลิตพลาสมาเย็นนี้ในทางปฏิบัติทำได้โดยใช้สนามไฟฟ้าเร่งอิเล็กตรอนให้มีพลังงานสูงมากพอและเข้าชนอะตอมหรือโมเลกุลของก๊าซแล้วทำให้ก๊าซเหล่านี้เกิดการแตกตัว (discharge) โดยที่อุณหภูมิของไอออนหรือกลุ่มก๊าซยังคงมีค่าใกล้เคียงกับอุณหภูมิห้อง ซึ่งโดยมากแล้วการผลิตพลาสมาเย็นจะใช้ก๊าซทำงานหรือก๊าซที่ป้อน (working or feed gas) เป็นก๊าซฮีเลียม (He) อาร์กอน (Ar) ไนโตรเจน (N2) หรือก๊าซผสมระหว่างก๊าซเหล่านี้กับก๊าซออกซิเจน (O2) อากาศ หรือไอน้ำในปริมาณเพียงเล็กน้อย[12,13] เพื่อให้ได้พลาสมาเย็นที่มีความหนาแน่นเพียงพอและมีอุณหภูมิต่ำ
การประยุกต์พลาสมาเย็นหรือพลาสมาอุณหภูมิต่ำความดันบรรยากาศ ด้วยปริมาณที่เหมาะสม (optimized dose) ได้รับการพิสูจน์แล้วว่ามีศักยภาพในการบำบัดแผลเรื้อรัง[1,6,14] เนื่องจากกระบวนการทางฟิสิกส์โดยเฉพาะการชนและปฏิกิริยาเคมีที่เกิดขึ้นระหว่างอิเล็กตรอนกับอนุภาคหรือระหว่างอนุภาคด้วยกันเองที่เกิดขึ้นในกลุ่มพลาสมาที่ถูกผลิตขึ้นในอากาศ[15,16] ซึ่งมีโมเลกุลของก๊าซไนโตรเจน (N2) ออกซิเจน (O2) และไอน้ำ (H2O) เป็นองค์ประกอบ รวมถึงปฏิกิริยาเคมีที่เกิดขึ้นระหว่างกลุ่มอนุภาคในพลาสมากับโมเลกุลน้ำที่อยู่บนแผลนั้นทำให้เกิดกลุ่มอนุมูลกลุ่มออกซิเจนและไนโตเจนไวต่อปฏิกิริยา (reactive oxygen and nitrogen species :RONS) [17–19] (โดยเป็นกลุ่มอนุมูลชนิดเดียวกันกับอนุมูลที่เกิดขึ้นเป็นปกติในร่างกายมนุษย์[20]) อนุมูล RONS ที่ถูกผลิตขึ้นโดยพลาสมาเย็นนี้ทำหน้าที่ในการบำบัดแผลเรื้อรังผ่านกระบวนการสำคัญ 2 อย่าง คือ การฆ่าเชื้อแบคทีเรีย (bactericidal) โดยสามารถฆ่าได้ทั้งแบคทีเรียแกรมบวก เช่น S. epidermidis และ S. aureus แบคทีเรียแกรมลบ เช่น E. coli และ P. aeruginosa และแบคทีเรียที่ดื้อยาปฏิชีวนะ เช่น vancomycin-resistant Enterococcus และ Methicillin-resistant Staphylococcus aureus (MRSA) [20,21] อนุมูลสำคัญที่มีบทบาทในด้านนี้ คือ อนุมูลไฮดรอกซิล (OH) อนุมูลออกไซด์ (O) โอโซน (O3) ไฮโดรเจนเปอร์ออกไซด์ (H2O2) ทำหน้าที่ในการทำลายผนังเซลล์ เยื้อหุ้มเซลล์ และ องค์ประกอบภายในเซลล์ เช่น DNA ของเซลล์แบคทีเรียด้วยกระบวนการการทำให้เกิดภาวะเครียดออกซิเดชั่น (oxidative stress) [22–25] นอกจากนี้ผลของการพลาสมาเย็นยังมีความจำเพาะ (selective) ต่อเซลล์แบคทีเรีย กล่าวคือ อนุมูลจากพลาสมาสามารถทำลายเซลล์แบคทีเรียโดยที่ไม่ทำให้เกิดความเสียหายแก่เซลล์หรือเนื้อเยื่อของแผล เนื่องจากเซลล์แบคทีเรียมีขนาดเล็กกว่าเซลล์มนุษย์มาก การทำลายเซลล์มนุษย์จึงต้องการปริมาณของอนุมูลจากพลาสมาที่สูงกว่าการฆ่าเซลล์แบคทีเรีย นอกจากนี้เซลล์มนุษย์ยังมีกลไกการซ่อมแซม DNA รวมถึงมีสารอนุมูลอิสระ (antioxidant) ที่เพียงพอในการปกป้องเซลล์[26] ในขณะที่อนุมูลไนตริกออกไซด์ (NO) ที่เกิดขึ้นจากพลาสมาเย็นนั้น เป็นอนุมูลที่ทำหน้าที่เป็นโมเลกุลส่งสัญญาณของเซลล์ (cell signaling molecule) ซี่งมีความเกี่ยวข้องกับระบบภูมิคุ้มกัน (immune system)[27] และมีผลต่อการกระตุ้นเซลล์ (cell stimulation) เช่น กระตุ้นการเพิ่มจำนวนของเซลล์ (cell proliferation) และการเคลื่อนที่ของเซลล์ (cell migration) การสร้างเส้นเลือดใหม่ (angiogenesis) รวมถึงการสังเคราะห์คอลลาเจน (collagen synthesis) เพื่อซ่อมแซมผิวหนังที่เสียหาย [1,6,28]

รูป 1 (ซ้าย) ระบบผลิตเจ็ตพลาสมาอากาศ (ขวา) เจ็ตพลาสมาอากาศ
ด้วยศักยภาพของพลาสมาเย็นความดันบรรยากาศที่มีต่อการบำบัดแผลดังที่อธิบายไปแล้วนั้น คณะผู้วิจัยของห้องปฏิบัติการพลาสมาไบโอ ศูนย์วิจัยฟิสิกส์ของพลาสมาและลำอนุภาค คณะวิทยาศาสตร์ มหาวิทยาลัยเชียงใหม่ จึงได้ทำการพัฒนาระบบผลิตเจ็ตพลาสมาอากาศ ดังแสดงในรูปที่ 1 (ซ้าย) โดยเป็นระบบที่กะทัดรัดที่มีปั๊มอากาศขนาดเล็กภายในเครื่อง ทำหน้าที่ดูดอากาศที่อยู่รอบตัวผ่านตัวกรองอากาศและส่งผ่านท่ออากาศไปยังหัวผลิตพลาสมา
เจ็ตพลาสมาอากาศ ดังแสดงในรูปที่ 1 (ขวา) เกิดขึ้นได้จากการให้ความต่างศักย์สูง (high voltage) ระหว่างขั้วอิเล็กโทรด 2 ขั้ว คือขั้วอิเล็กโทรดศักย์สูง (high-voltage electrode) และอิเล็กโทรดศักย์ศูนย์ (grounded electrode) เมื่อขนาดของความต่างศักย์นี้มีค่าเพิ่มขึ้นจนเท่ากับศักย์ไฟฟ้าแตกตัว (breakdown voltage, Vb) ของอากาศ จะทำให้เกิดการดิสชาร์จของอากาศขึ้นระหว่างปลายของแท่งอิเล็กโทรดศักย์สูงกับผิวด้านในของอิเล็กโทรดศักย์ศูนย์ โดยมีเป็นลักษณะการดิสชาร์จเป็น transient spark discharge ที่ประกอบด้วย 2 เฟสสำคัญ คือ streamer discharge และ spark discharge [29,30] ซึ่งการดิสชาร์จนี้มีลักษณะเฉพาะคือ ทำให้เกิดกระแสไฟฟ้าของการดิสชาร์จ (discharge current) ขนาดมากกว่า 0.1 แอมแปร์ในเวลาสั้นมาก ๆ ในระดับ 10 นาโนวินาที ถึง 5 ไมโครวินาที การทำให้กระแสไฟฟ้าของการดิสชาร์จที่มีค่ามากกว่า 0.1 แอมแปร์ ทำให้อิเล็กตรอนมีจำนวนมากและมีพลังงานสูงเพียงพอต่อการทำให้โมเลกุลไนโตรเจน ออกซิเจน และไอน้ำ เกิดปฏิกิริยาการแตกตัวเป็นไอออน อะตอม และโมเลกุล และปฏิกิริยาที่เกิดขึ้นในกลุ่มไอออน อะตอม โมเลกุลเหล่านี้ทำให้เกิดกลุ่มอนุมูลออกซิเจนและไนโตรเจนที่ไวต่อปฏิกิริยา แต่เนื่องจากกระแสไฟฟ้าของการดิสชาร์จนี้เกิดขึ้นในเวลาที่สั้นมาก ๆ ระดับ 10 นาโนวินาที ถึง 5 ไมโครวินาทีนี้ ทำให้จำนวนของการชนระหว่างอิเล็กตรอนกับกลุ่มอนุมูลที่มีมวลมาก (ไอออน อะตอม และโมเลกุล) มีจำนวนน้อยครั้ง การถ่ายทอดพลังงานจากอิเล็กตรอนไปสู่กลุ่มอนุมูลที่มีมวลมากจึงเกิดได้น้อยและทำให้อนุมูลที่มีมวลมากเหล่านี้ไม่อยู่ในสมดุลความร้อนกับอิเล็กตรอน อนุมูลที่มีมวลมากเหล่านี้จึงยังมีอุณหภูมิใกล้เคียงกับอากาศที่ป้อนเข้าไป หลังจากนั้นกลุ่มพลาสมาอากาศที่ถูกผลิตขึ้นจะออกมาทางรูเปิดที่แคบด้วยการการไหลของอากาศ (air flow) ให้มีรูปร่างเป็นลำเจ็ตหรือรูปร่างคล้ายเข็ม โดยคณะผู้วิจัยได้พัฒนาให้เกิดการดิสชาร์จของพลาสมาอากาศในแบบกลุ่มพัลส์ไฟฟ้ากระแสตรง โดยแต่ละพัลส์มีความกว้างในระดับ 10 นาโนวินาที ถึง 5 ไมโครวินาที จำนวนหลายๆ พัลส์แต่ไม่เกิน 10 พัลส์ต่อกลุ่ม เรียกรูปแบบการดิสชาร์จลักษณะนี้ว่า burst mode ซึ่งมีข้อดีกว่าการใช้ไฟฟ้าศักย์สูงคลื่นรูปไซน์ (sinusoidal waveform) ที่มีลักษณะการให้พลังงานแก่พลาสมาแบบต่อเนื่องอันจะทำให้พลาสมาอากาศที่ได้มีอุณหภูมิสูง ซึ่งไม่เหมาะสำหรับการใช้งานในทางชีววิทยาศาสตร์
จากการวิเคราะห์แสงที่เปล่งออกจากกลุ่มเจ็ตพลาสมาอากาศด้วยสเปกโทรสโคปีแบบเปล่งแสง (OES) ดังแสดงในรูปที่ 2 ทำให้เห็นได้อย่างชัดเจนว่าเจ็ตพลาสมาอากาศนั้นประกอบด้วยอนุมูลที่มีบทบาทสำคัญต่อการบำบัดแผลเรื้อรัง ได้แก่ อนุมูลไฮดรอกซิล (OH) และ อนุมูลออกไซด์ (O) นอกจากนี้อะตอมหรือโมเลกุล N, O, H, OH ที่ปรากฏให้เห็นยังสามารถทำปฏิกิริยาเคมีกับโมเลกุลก๊าซไนโตรเจนและออกซิเจน หรือ ทำปฏิกิริยาระหว่างกันเองทำให้เกิดอนุมูลไนตริกออกไซด์ (NO) และโอโซน (O3) [17]

รูปที่ 2 สเปกตรัมของแสงที่เปล่งออกจากเจ็ตพลาสมาอากาศ

รูปที่ 3 อัตราการเกิดอนุมูลไนตริกออกไซด์และโอโซนในเจ็ตพลาสมาอากาศโดยเป็นฟังก์ชันของจำนวนพัลส์ต่อกลุ่ม
การทดสอบด้วยก๊าซเซนเซอร์พบว่าเจ็ตพลาสมาอากาศสามารถผลิตอนุมูลไนตริกออกไซด์และโอโซนดังแสดงในรูปที่ 3 โดยเกิดอนุมูลไนตริกออกไซด์ในปริมาณที่มากกว่าอนุมูลโอโซนเป็นอย่างมาก ซึ่งโอโซนที่เกิดเพียงเล็กน้อยนี้มีประโยชน์อย่างมากต่อการฆ่าเชื้อแบคทีเรียที่อยู่บนแผลและมีโอกาสน้อยมากที่จะฟุ้งกระจายสู่อากาศโดยรอบ นอกจากนี้อนุมูลต่าง ๆ ที่อยู่ในเจ็ตพลาสมาโดยเฉพาะโอโซนนั้นเมื่อสัมผัสกับโมเลกุลน้ำที่อยู่บริเวณแผลจะทำให้เกิดไฮโดรเจนเปอร์ออกไซด์ (H2O2) และการทดสอบการฆ่าเชื้อแบคทีเรียดื้อยา MRSA ด้วยเจ็ตพลาสมาอากาศดังแสดงในรูปที่ 4 แสดงให้เห็นถึงศักยภาพของเจ็ตพลาสมาอากาศในการช่วยบำบัดแผลติดเชื้อเรื้อรังโดยการฆ่าแบคทีเรียในแผล

รูปที่ 4 ผลของเจ็ตพลาสมาอากาศต่อการฆ่าเชื้อแบคทีเรียดื้อยา MRSA
จะเห็นได้ว่าระบบผลิตเจ็ตพลาสมาอากาศเป็นนวัตกรรมที่สามารถเปลี่ยนอากาศที่อยู่รอบตัวเรา ให้เป็นสิ่งที่ช่วยบำบัดแผลติดเชื้อที่รักษาด้วยวิธีการปกติได้ยากและนำไปสู่เชื้อโรคดื้อยา ให้หายเร็วขึ้น และใช้ต้นทุนการผลิตพลาสมาเย็นที่ต่ำมาก คือ ใช้อากาศที่เราหายใจ และพลังงานไฟฟ้าด้วยต้นทุนเพียง 1.8 บาทต่อการรักษาหนึ่งคนในหนึ่งเดือน (วันละ 20 นาที จำนวน 30 วัน)

รูปที่ 5 ตัวอย่างแผลเรื้อรังที่เท้าจากโรคหลอดเลือดดํา (Venous Ulcer) และ แผลเนื้อเน่า (Necrotizing Fasciitis) ที่ผ่านการบำบัดด้วยเจ็ตพลาสมาอากาศเป็นเวลา 5 สัปดาห์
เรียบเรียงโดย
พุฒิธร ธะนะ
ภาควิชาฟิสิกส์และวัสดุศาสตร์ คณะวิทยาศาสตร์ มหาวิทยาลัยเชียงใหม่
รศ.ดร.ธีรวรรณ บุญญวรรณ
ภาควิชาฟิสิกส์และวัสดุศาสตร์ คณะวิทยาศาสตร์ มหาวิทยาลัยเชียงใหม่
อ้างอิง
-
[1] Haertel B, von Woedtke T, Weltmann K-D and Lindequist U 2014 Non-thermal atmospheric-pressure plasma possible application in wound healing. Biomol. Ther. (Seoul). 22 477–90
-
[2] Clinton A and Carter T 2015 Chronic Wound Biofilms: Pathogenesis and Potential Therapies Lab. Med. 46 277–84
-
[3] Nunan R, Harding K G and Martin P 2014 Clinical challenges of chronic wounds: searching for an optimal animal model to recapitulate their complexity Dis. Model. Mech. 7 1205–13
-
[4] Zhao G, Usui M L, Lippman S I, James G A, Stewart P S, Fleckman P and Olerud J E 2013 Biofilms and Inflammation in Chronic Wounds Adv. Wound Care 2 389–99
-
[5] Frykberg R G and Banks J 2015 Challenges in the Treatment of Chronic Wounds. Adv. wound care 4 560–82
-
[6] Graves D B 2012 The emerging role of reactive oxygen and nitrogen species in redox biology and some implications for plasma applications to medicine and biology J. Phys. D. Appl. Phys. 45 263001
-
[7] Thiruvoth F, Mohapatra D, Sivakumar D, Chittoria R and Nandhagopal V 2015 Current concepts in the physiology of adult wound healing Plast. Aesthetic Res. 2 250
-
[8] Tsourdi E, Barthel A, Rietzsch H, Reichel A and Bornstein S R 2013 Current Aspects in the Pathophysiology and Treatment of Chronic Wounds in Diabetes Mellitus Biomed Res. Int. 2013 1–6
-
[9] Demidova-Rice T N, Hamblin M R and Herman I M 2012 Acute and Impaired Wound Healing Adv. Skin Wound Care 25 304–14
-
[10] Robson M C 2004 Pathophysiology of Chronic Wounds Surgery in Wounds (Berlin, Heidelberg: Springer Berlin Heidelberg) pp 29–40
-
[11] Weltmann K-D and von Woedtke T 2011 Basic requirements for plasma sources in medicine Eur. Phys. J. Appl. Phys. 55 13807
-
[12] Kong M G, Kroesen G, Morfill G, Nosenko T, Shimizu T, van Dijk J and Zimmermann J L 2009 Plasma medicine: an introductory review New J. Phys. 11 115012
-
[13] Lu X, Naidis G V, Laroussi M, Reuter S, Graves D B and Ostrikov K 2016 Reactive species in non-equilibrium atmospheric-pressure plasmas: Generation, transport, and biological effects Phys. Rep. 630 1–84
-
[14] Metelmann H, Woedtke T von and Weltmann K 2018 Comprehensive Clinical Plasma Medicine ed H-R Metelmann, T von Woedtke and K-D Weltmann (Cham: Springer International Publishing)
-
[15] Meichsner, J., Schmidt, M., Schneider, R., Wagner H E 2013 Nonthermal Plasma Chemistry and Physics ed H-E Wagner (CRC Press)
-
[16] Fridman A and Kennedy L A 2004 Plasma Physics and Engineering (Abingdon, UK: Taylor & Francis)
-
[17] Dorai R and Kushner M J 2003 A model for plasma modification of polypropylene using atmospheric pressure discharges J. Phys. D. Appl. Phys. 36 666–85
-
[18] Nikiforov A, Li L, Britun N, Snyders R, Vanraes P and Leys C 2014 Influence of air diffusion on the OH radicals and atomic O distribution in an atmospheric Ar (bio)plasma jet Plasma Sources Sci. Technol. 23 015015
-
[19] Anderson C E, Cha N R, Lindsay A D, Clark D S and Graves D B 2016 The Role of Interfacial Reactions in Determining Plasma–Liquid Chemistry Plasma Chem. Plasma Process. 36 1393–415
-
[20] Weltmann K-D and von Woedtke T 2017 Plasma medicine—current state of research and medical application Plasma Phys. Control. Fusion 59 014031
-
[21] O’Connor N, Cahill O, Daniels S, Galvin S and Humphreys H 2014 Cold atmospheric pressure plasma and decontamination. Can it contribute to preventing hospital-acquired infections? J. Hosp. Infect. 88 59–65
-
[22] Han L, Patil S, Boehm D, Milosavljević V, Cullen P J and Bourke P 2016 Mechanisms of Inactivation by High-Voltage Atmospheric Cold Plasma Differ for Escherichia coli and Staphylococcus aureus ed E G Dudley Appl. Environ. Microbiol. 82 450–8
-
[23] Fridman A and Friedman G Plasma Medicine (Hoboken, NJ, USA: John Wiley & Sons, Inc.)
-
[24] Misra N N, Schlüter O and Cullen P J 2016 Plasma in Food and Agriculture Cold Plasma in Food and Agriculture vol 44 (Elsevier) pp 1–16
-
[25] Bandyopadhyay U, Das D and Banerjee R K 1999 Reactive oxygen species : Oxidative damage and pathogenesis Current 77 658–66
-
[26] Dobrynin D, Fridman G, Friedman G and Fridman A 2009 Physical and biological mechanisms of direct plasma interaction with living tissue New J. Phys. 11 115020
-
[27] Villalobo A 2006 Nitric oxide and cell proliferation. FEBS J. 273 2329–44
-
[28] Suschek C V. and Opländer C 2016 The application of cold atmospheric plasma in medicine: The potential role of nitric oxide in plasma-induced effects Clin. Plasma Med. 4 1–8
-
[29] Janda M, Martišovitš V and Machala Z 2011 Transient spark: a dc-driven repetitively pulsed discharge and its control by electric circuit parameters Plasma Sources Sci. Technol. 20 035015
-
[30] Janda M, Machala Z, Niklová A and Martišovitš V 2012 The streamer-to-spark transition in a transient spark: a dc-driven nanosecond-pulsed discharge in atmospheric air Plasma Sources Sci. Technol. 21 045006
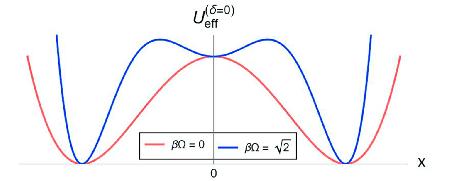 ฟิสิกส์ของปฏิสัมพันธ์ระหว่าง แมว กับคน … เมื่อน้องแมวถูกนำมาช่วยสอนฟิสิกส์ ( พฤติกรรมที่น่าฉงน และบทสรุป )
18-03-2025
ฟิสิกส์ของปฏิสัมพันธ์ระหว่าง แมว กับคน … เมื่อน้องแมวถูกนำมาช่วยสอนฟิสิกส์ ( พฤติกรรมที่น่าฉงน และบทสรุป )
18-03-2025
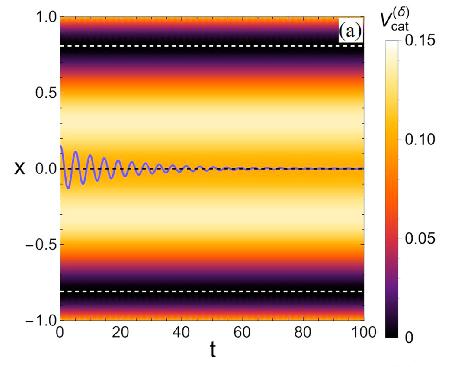 ฟิสิกส์ของปฏิสัมพันธ์ระหว่าง แมว กับคน … เมื่อน้องแมวถูกนำมาช่วยสอนฟิสิกส์ ( ตอนที่ 2: คำอธิบายพฤติกรรมหลัก )
18-03-2025
ฟิสิกส์ของปฏิสัมพันธ์ระหว่าง แมว กับคน … เมื่อน้องแมวถูกนำมาช่วยสอนฟิสิกส์ ( ตอนที่ 2: คำอธิบายพฤติกรรมหลัก )
18-03-2025
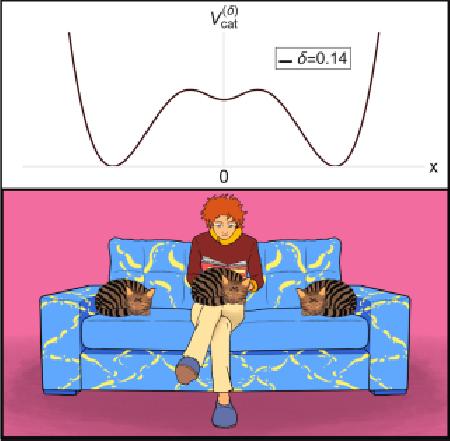 ฟิสิกส์ของปฏิสัมพันธ์ระหว่าง แมว กับคน … เมื่อน้องแมวถูกนำมาช่วยสอนฟิสิกส์ ( ตอนที่ 1: เกริ่นนำ )
17-03-2025
ฟิสิกส์ของปฏิสัมพันธ์ระหว่าง แมว กับคน … เมื่อน้องแมวถูกนำมาช่วยสอนฟิสิกส์ ( ตอนที่ 1: เกริ่นนำ )
17-03-2025
 หรือว่าเราอาศัยอยู่ในโฮโลแกรม ?
24-10-2024
หรือว่าเราอาศัยอยู่ในโฮโลแกรม ?
24-10-2024

